Фенотиазин :: Химические свойства
Фенотиазин · Получение · Физические свойства · Химические свойства · Физиологическое действие · Производные фенотиазина · Обнаружение и определение · Примечания ·
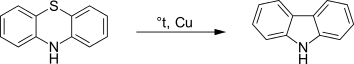
При нагревании с медью фенотиазин отщепляет атом серы, переходя помимо этого в карбазол:
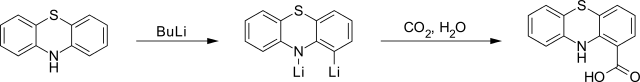
При обработке бутиллитием фенотиазин даёт 1,10-дилитийпроизводное, при карбоксилировании которого образуется фенотиазинкарбоновая-1 кислота:
Окисление
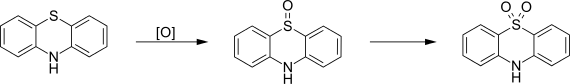
Фенотиазин проявляет восстановительные свойства. Под воздействием перманганата калия и перекиси водорода происходит окисление по атому серы с образованием неустойчивого, легко восстанавливающегося до фенотиазина фенотиазиноксида-5 и более устойчивого фенотиазиндиоксида-5,5:
При взаимодействии с другими окислителями (серная кислота, Fe(III), Ce(IV)) происходит С-окисление в положения 3 и 7:
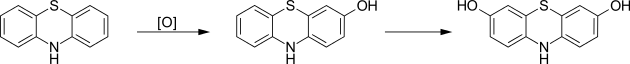
Электрофильное замещение
Будучи ароматическим соединением, фенотиазин является донором электронов и легко вступает в реакции электрофильного замещения.
Хлорирование фенотиазина в среде уксусной кислоты приводит к замещению хлором атомов водорода сначала в положениях 3 и 7, а после 1 и 9. Конечным продуктом хлорирования является 1,3,7,9-тетрахлорфенотиазин:
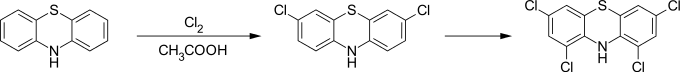
При хлорировании в среде нитробензола происходит глубокое хлорирование с присоединением до 11 атомов хлора и потерей ароматичности одного из колец:
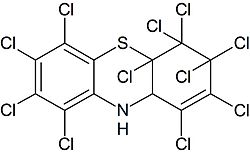
При нагревании до 180°С этот продукт ощепляет три атома хлора, помимо этого образуется устойчивый свободный радикал, который частично димеризуется, в результате чего образуется 10,10'-би-(октахлорфенотиазинил).
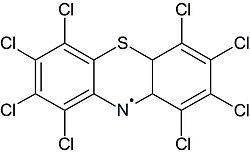
Соотношение свободного радикала и 10,10'-би-(октахлорфенотиазинил)а при температуре 180°С составляет 30:70.
При бромировании фенотиазина в уксусной кислоте последовательно образуются 3,7-, 1,3,7- и 1,3,7,9-бромпроизводные. Бромирование в среде нитробензола приводит к образованию 1,2,3,7,8,9-гексабромфенотиазина.
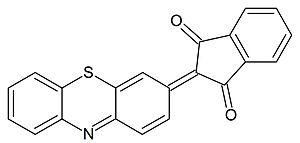
При окислении фенотиазина хлоридом железа (III) в присутствии п-толуолсульфоната натрия, нитрита натрия или тиомочевины образуются следовательно 3-(п-толуолсульфонил)фенотиазин и 3-нитрофенотиазин, а после гидролиза изотиурониевой соли — 3-меркаптофенотиазин. В присутствии соединений, содержащими активные метиленовые группы, образуются красители с хиноидной структурой, к примеру, в результате взаимодействия с индандионом-1,3:
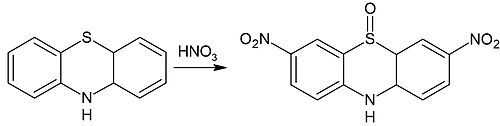
Электрофильное замещение в фенотиазине может также сопровождаться окислением. Так, конечным продуктом нитрования фенотиазина азотной кислотой является 3,7-динитрофенотиазиноксид-5:
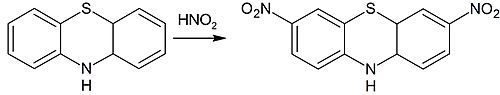
а нитрование азотистой кислотой приводит к 3,7-динитрофенотиазину:
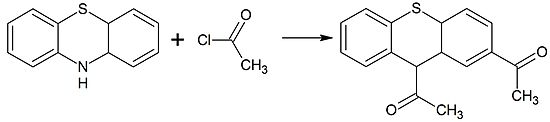
Ацилирование фенотиазина по Фриделю-Крафтсу приводит в основном к замещению в положения 2,10, в тоже время выделены также продукты реакции неустановленного состава:
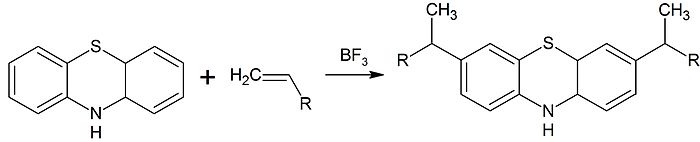
Фенотиазин сульфируется хлорсульфоновой кислотой. Алкилирование фенотиазина алкенами в присутствии трифторида бора приводит к 3,7 диалкилпроизводным:
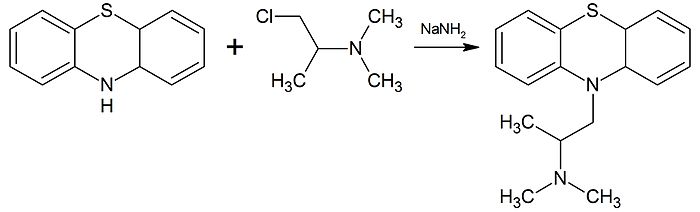
При взаимодействии фенотиазина с хлорзамещёнными третичными и вторичными аминами в присутствии амида натрия образуются 10-замещённые производные фенотиазина. К примеру, при алкилировании фенотиазина 2-диметиламино-1-хлорпропаном или 1-диметиламино-2-хлорпропаном образуется 10-(2-диметиламинопропил)фенотиазин (прометазин):
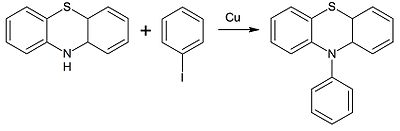
Фенотиазин вступает в реакцию Ульмана, при нагревании с металлической медью и иодбензолом в среде нитробензола, толуола или ДМФА присоединение бензольного кольца происходит в положение 10 с образованием 10-фенилфенотиазина:
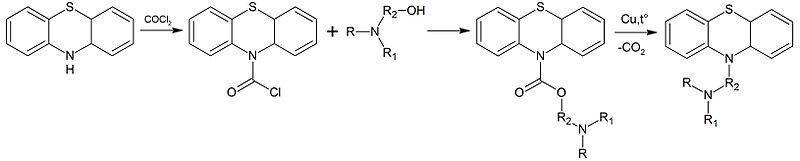
При взаимодействии фенотиазина с фосгеном образуется 10-хлоркарбонилфенотиазин, при реакции с аминоспиртами образующий сложные эфиры, которые при нагревании в вакууме с медью отщепляют углекислый газ, что даёт возможность вводить чувствительные к щелочам группы: