Гидроксид натрия
Гидроксид натрия · Физические свойства · Химические свойства · Качественное определение ионов натрия · Методы получения · Рынок каустической соды · Применение · Меры предосторожности при обращении с гидроксидом натрия · Литература ·
| Гидроксид натрия | |
 | |
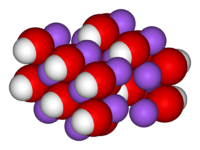 | |
| Общие | |
|---|---|
| Традиционные названия | едкий натр, каустик, каустическая сода, едкая щелочь |
| Хим. формула | NaOH |
| Физические свойства | |
| Молярная масса | 39,997 г/моль |
| Плотность | 2,13 г/см |
| Термические свойства | |
| Т. плав. | 323 °C |
| Т. кип. | 1403 °C |
| Химические свойства | |
| Растворимость в воде | 108,7 г/100 мл |
| Классификация | |
| Рег. номер CAS | |
| PubChem | |
| SMILES |
|
| ChemSpider | |
| Безопасность | |
| Токсичность |
 0
3
1
ALK |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иначе. | |
Гидроксид натрия (латынь Natrii hydroxidum; другие названия — каустическая сода, каустик, едкий натр, едкая щёлочь) — самая распространённая щёлочь, химическая формула NaOH. В год в мире производится и потребляется более 57 миллионов тонн едкого натра.
Интересна история тривиальных названий как гидроксида натрия, так и других щелочей, название «едкая щёлочь» обусловлено свойством разъедать кожу, бумагу, и прочие органические вещества, вызывая сильные ожоги. До XVII века щёлочью (фр. alkali) называли также карбонаты натрия и калия. В 1736 г. французский учёный А. Л. Дюамель дю Монсо впервые различил эти вещества: гидроксид натрия стали называть каустической содой, карбонат натрия — кальцинированной содой (по растению Salsola Soda из рода Солянка, из золы которого её добывали), а карбонат калия — поташем. Сегодня содой принято называть натриевые соли угольной кислоты. В английском и французском языках слово sodium означает натрий, potassium — калий.