Карбоновые кислоты :: Физические свойства
Карбоновые кислоты · Номенклатура · Классификация · История открытия · Нахождение в природе · Получение · Физические свойства · Строение · Сила · Карбоновые кислотные остатки · Характерные химические реакции и получение важных производных · Химические методы анализа карбоновых кислот · Спектральные методы анализа карбоновых кислот · Применение · Литература · Официальный сайт · Примечания · Близкие статьи ·
Низшие кислоты с числом атомов углерода до 3 - легкоподвижные бесцветные жидкости с характерным резким запахом, смешиваются с водой в любых соотношениях. Большая часть кислот с 4-9 атомами карбона - маслянистые жидкости с неприятным запахом. Кислоты с большим количеством атомов карбона - твёрдые вещества, нерастворимые в воде. Плотность муравьиной и уксусной кислот больше единицы, остальных - меньше. Температура кипения возрастает по мере увеличения молекулярной массы, при одном и том же числе углеродных атомов кислоты нормального строения кипят при более высокой температуре, чем кислоты изостроения.
У кислот нормального строения есть закономерность: температура плавления кислот с чётным числом атомных углеродов выше, чем температура плавления соседних с нечётным числом. Это объясняется расположением метильной и карбоксильной групп - в кислотах чётного ряда они по разные стороны от оси молекулы, а нечётного - по разные. Благодаря более симметричному строению молекулы кислоты с чётным числом атомов углерода сильнее взаимодействуют между собой в кристаллической решётке и её труднее разрушить при нагревании.
Карбоновые кислоты кипят при значительно более высоких температурах, чем спирты. Их молекулы ассоциированы намного сильнее вследствие того что связи 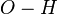 в них в большей степени поляризованы по типу
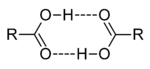
в них в большей степени поляризованы по типу 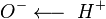 . Кроме того, у карбоновых кислот имеется возможность образования водородных связей с кислородом карбонильного диполя, обладающим значительной электроотрицательностью, а не только с кислородом другой гидроксильной группы. Действительно, в твердом состоянии карбоновые кислоты существуют в основном в виде циклических димеров, а в жидком происходит и линейная асоциация. Даже в парах они димеризированы. Две водородные связи довольно прочны, энергия димеризации для муравьиной кислоты составляет 14 ккал/моль.
. Кроме того, у карбоновых кислот имеется возможность образования водородных связей с кислородом карбонильного диполя, обладающим значительной электроотрицательностью, а не только с кислородом другой гидроксильной группы. Действительно, в твердом состоянии карбоновые кислоты существуют в основном в виде циклических димеров, а в жидком происходит и линейная асоциация. Даже в парах они димеризированы. Две водородные связи довольно прочны, энергия димеризации для муравьиной кислоты составляет 14 ккал/моль.