Индольные алкалоиды :: Биосинтез
Индольные алкалоиды · История · Классификация · Неизопреноидные индольные алкалоиды · Изопреноидные индольные алкалоиды · Бисиндольные алкалоиды · Распространение в природе · Биосинтез · Физиологическая активность · Применение · Примечания · Литература ·
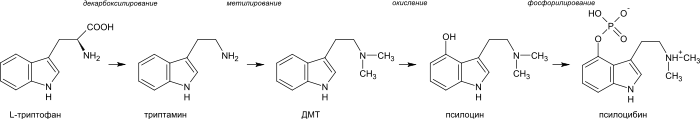
Биогенетическим предшественником всех индольных алкалоидов является аминокислота триптофан. Для большинства из них первым шагом является декарбоксилирование триптофана с образованием триптамина. Диметилтриптамин (ДМТ) образуется из триптамина посредством метилирования при участии кофермента S-аденозилметионина (SAM). Псилоцин образуется из диметилтриптамина посредством окисления и далее фосфорилируется до псилоцибина.
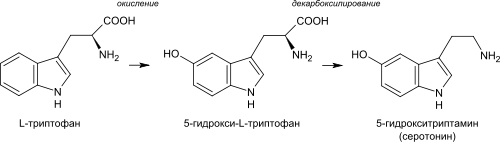
При биосинтезе серотонина промежуточным соединением является не триптамин, а 5-гидрокситриптофан, который уже в свою очередь декарбоксилируется с образованием 5-гидрокситриптамина (серотонина).
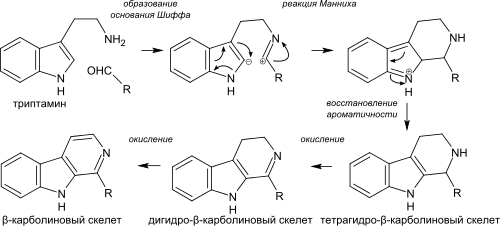
Биосинтез -карболиновых алкалоидов происходит посредством образования основания Шиффа из триптамина и альдегида (или кетокислоты) и последующей внутримолекулярной реакции Манниха, где атом углерода C2 индольного ядра выступает в роли нуклеофила. После этого ароматичность восстанавливается с потерей протона при атоме углерода C2. Получившийся тетрагидро--карболиновый скелет после последовательно окисляется до дигидро--карболинового и -карболинового. При образовании простых -карболиновых алкалоидов, таких как гармин и гармалин роль кетокислоты выполняет пировиноградная кислота. При синтезе монотерпеноидных индольных алкалоидов в качестве альдегида участвует скологанин. Пирролоиндольные алкалоиды синтезируются в живых организмах аналогичным способом.
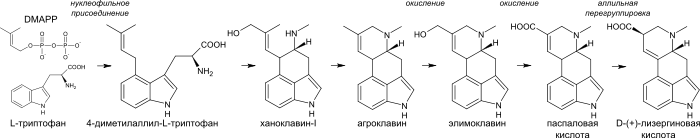
Биосинтез алкалоидов спорыньи начинается с алкилирования триптофана диметилаллилпирофосфатом (англ. Dimethylallyl pyrophosphate), помимо этого атом углерода C4 индольного ядра играет роль нуклеофила. Образовавшийся 4-диметилаллил-L-триптофан подвергается N-метилированию. Дальнейшими ступенями биосинтеза являются ханоклавин-I и агроклавин. Последний гидроксилируется до элимоклавина, который в свою очередь окисляется до паспаловой кислоты. В процессе аллильной перегруппировки паспаловая кислота преобразуется в лизергиновую кислоту.
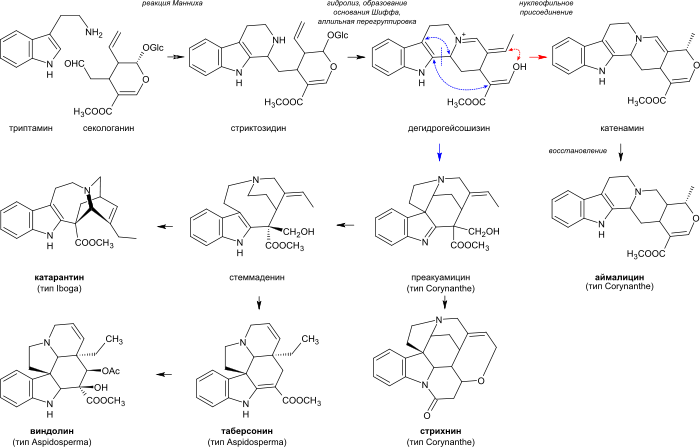
Биосинтез монотерпеноидных индольных алкалоидов начинается реакцией Манниха с участием триптамина и секологанина, в результате которой образуется стриктозидин, преобразуемый далее в 4,21-дегидрогейсошизин. Далее биосинтез большинства алкалоидов с неперегруппированной монотерпеноидной частью (типа Corynanthe) продолжается посредством циклизации с образованием катенамина и последующего восстановления до аймалицина в присутствии никотинамидадениндинуклеотидфосфата (NADPH). При биосинтезе других алкалоидов 4,21-дегидрогейсошизин сначала преобразуется в преакуамицин, алкалоид подтипа Strychnos типа Corynanthe, из которого в свою очередь образуются другие алкалоиды подтипа Strychnos, и кроме этого алкалоиды типов Iboga и Aspidosperma. Бисиндольные алкалоиды винбластин и винкристин получаются в процессе реакции, вовлекающей катарантин (алкалоид типа Iboga) и виндолин (алкалоид типа Aspidosperma).